Neuropatologia
TECIDO NERVOSO NORMAL
O sistema nervoso central (SNC) é constituído por células especializadas para geração e transmissão de impulsos elétricos, os neurônios, e pelas células da glia, que têm diferentes funções conforme o seu tipo.
NEURÔNIOS
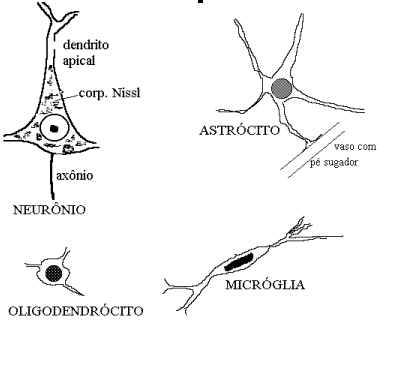
Os neurônios têm forma e tamanho variados de acordo com sua localização e função. Mostram em HE núcleo redondo, vesiculoso, com nucléolo nítido. O citoplasma é abundante e possue corpúsculos basófilos, os corpúsculos de Nissl ou substância tigróide, constituídos por retículo endoplásmico rugoso responsável por síntese proteica.Os neurônios sintetizam proteínas em abundância, sendo parte estruturais (constituintes de membranas e organelas) e parte enzimas necessárias, entre outras funções, à síntese e liberação de neurotransmissores. Quanto maior o corpo celular, mais nítidos são os corpúsculos de Nissl.
No citoplasma dos neurônios há também neurofibrilas, demonstráveis com impregnação pela prata e constituídas por microtúbulos e neurofilamentos. São responsáveis pelo transporte de substâncias do corpo celular aos prolongamentos e vice-versa (transporte axonal).
Todos neurônios possuem um único axônio ou cilindro-eixo, o prolongamento responsável pela transmissão de impulsos a outros neurônios ou a órgãos efetores. Tem diâmetro constante e suas ramificações ocorrem próximas à extremidade distal.
Além do axônio, o corpo celular pode ter dendritos, que se ramificam já a curta distância. Sua função é ampliar a superfície da célula e receber contatos sinápticos. Corpúsculos de Nissl são encontrados na porção proximal dos dendritos, mas nunca no axônio. Há neurônios sem dendritos, p. ex., neurônios sensitivos nos gânglios de raiz posterior, cujo corpo celular tem forma globosa. Contudo não há neurônios sem axônio.
Os maiores neurônios são as células piramidais de Betz do córtex cerebral motor (área 4 de Brodmann, giro pré-central), cujos axônios vão até a medula espinal, e os motoneurônios dos cornos anteriores da medula, cujos axônios atingem até músculos das mãos e pés. As células de Purkinje do cerebelo também são grandes, com corpo celular em forma de taça e um dendrito apical ricamente arborizado. Ainda no córtex cerebelar temos os menores neurônios do corpo, as células granulosas, cujo núcleo, ao contrário do dos outros neurônios, é pequeno e denso, semelhante a um linfócito, não se reconhecendo nucléolo. Em suma, para reconhecimento dos neurônios baseamo-nos no núcleo redondo, com cromatina frouxa e nucléolo evidente e no citoplasma, basófilo e de limites nítidos. (Os corpúsculos de Nissl são bem distintos só nos neurônios maiores.
NEURÔNIOS MORFOLOGIA
Corpo Celular: Núcleo: redondo, cromatina frouxa, nucléolo bem nítido.
Citoplasma: basófilo (roxo em HE), distinto, limites precisos. Em neurônios maiores: corpúsculos de Nissl.
PROLONGAMENTOS
Axônio: Único em qualquer neurônio. Diâmetro constante. Ramificações próximas à extremidade distal. Revestido por baínha de mielina.
Dendritos: Número variável. Podem não existir. Diâmetro decresce à medida que o dendrito se ramifica. Nunca apresentam mielina.
CÉLULAS DA GLIA
Morfologia normal na HE. As células da glia normais têm citoplasma não visível na HE, sendo reconhecidas pela morfologia do núcleo. Para demonstrar-se o citoplasma das células da glia e seus prolongamentos são usadas técnicas especiais.Os astrócitos e oligodendrócitos têm núcleo redondo menor que o do neurônio e sem nucléolo perceptível. O do astrócito é maior e mais frouxo que o do oligodendrócito; o núcleo deste último lembra o de um linfócito. Já a micróglia tem núcleo pequeno, alongado em forma de vírgula, com cromatina densa, também sem nucléolo.
ASTRÓCITOS
Com técnicas especiais (impregnação argêntica), os astrócitos mostram-se de dois tipos: protoplasmáticos e fibrosos. Os primeiros predominam na substância cinzenta e os segundos na branca. Os astrócitos protoplasmáticos têm prolongamentos mais numerosos, curtos, delicados e ramificados que os dos astrócitos fibrosos. Muitos prolongamentos dos dois tipos de astrócito terminam em vasos sangüíneos por uma expansão à maneira de trombeta, o pé sugador (nome equivocado, pois os astrócitos não sugam vasos).
As funções dos astrócitos são muitas:
1. Sustentação mecânica do tecido nervoso. Ambos tipos de astrócito contêm no citoplasma filamentos intermediários constituídos por vimentina e por uma proteína exclusiva, a proteína glial fibrilar ácida (glial fibrillary acidic protein ou GFAP). Estes filamentos denominam-se fibrilas gliais e podem ser demonstradas por imunohistoquímica. As fibrilas gliais têm função de sustentação mecânica: os astrócitos e seus prolongamentos constituem uma trama ancorada nos vasos, na qual se apóiam os neurônios e outras células.
2. Os prolongamentos astrocitários recobrem a superfície externa dos vasos, desde artérias e veias até capilares. Sugere-se que teriam papel na constituição da barreira hemo-encefálica.
3. Na substância cinzenta os prolongamentos dos astrócitos protoplasmáticos envolvem os neurônios, mantendo um microambiente adequado às funções metabólicas destes. P. ex., a atividade neuronal causa aumento na concentração extracelular de potássio; o excesso deste íon seria captado pelos astrócitos.
4. Os prolongamentos dos astrócitos protoplasmáticos funcionariam como isolantes elétricos de certas sinapses, impedindo que a difusão de neurotransmissores excite indesejavelmente sinapses vizinhas.
5. É possível que astrócitos captem neurotransmissores liberados e facilitem o retorno dos precursores aos neurônios para reutilização.
6. As funções dos astrócitos na cicatrização do tecido nervoso serão descritas abaixo.
OLIGODENDRÓGLIA: A oligodendróglia em impregnações argênticas mostra corpo celular arredondado e pequeno e poucos prolongamentos, curtos, finos e pouco ramificados (daí o nome: óligo – pouco; dendro – ramificação). Estas células são responsáveis pela formação e manutenção das baínhas de mielina para os axônios do SNC, função que nos nervos periféricos é desempenhada pelas células de Schwann. Cada prolongamento de um oligodendrócito forma um internodo de mielina: expande-se à maneira de uma pá e enrola-se em volta do axônio sucessivas vezes, lembrando um rolo de papel. O espaço entre dois internodos é o nodo de Ranvier, onde se dão as trocas iônicas da condução saltatória. Cada oligodendrócito pode formar até 50 internodos de mielina em axônios próximos.
MICRÓGLIA
A micróglia impregnada pela prata apresenta citoplasma escasso formando delgados prolongamentos a partir das extremidades da célula, que se ramificam dicotomicamente. A única função reconhecida da micróglia é reagir a lesões do tecido nervoso fagocitando restos celulares.
NEURONIOS E GLIA
ALTERAÇÕES PATOLÓGICAS DOS NEURÔNIOS
1.Necrose. Praticamente todas as alterações patológicas dos neurônios são regressivas e a mais importante é a necrose. A causa mais comum é anóxia, geralmente por isquemia, daí o termo alteração celular isquêmica. O neurônio necrótico tem volume diminuído, núcleo picnótico e ovalado ou cariolítico. O citoplasma perde a basofilia normal e os corpúsculos de Nissl, passando a eosinófilo. Esses caracteres são os mesmos de qualquer outra célula necrótica. O neurônio necrótico pode sofrer lise ou, mais raramente, pode calcificar-se mantendo a silhueta do corpo celular e dos dendritos.
2.Retração. A retração celular é uma alteração comum, em que o neurônio diminue de volume, o núcleo torna-se picnótico e o citoplasma mais basófilo que o normal. Esta alteração pode representar grave lesão celular, mas o mesmo aspecto pode também ser produzido por manipulação do tecido nervoso a fresco e corresponder, portanto, a artefato. Daí a cautela necessária em sua interpretação.
3.Atrofia. Como outras células, o neurônio pode sofrer redução do volume celular, atingindo principalmente o citoplasma. Esse processo de atrofia simples é de evolução lenta e observado em várias doenças degenerativas do SNC, como a esclerose lateral amiotrófica. Nesta doença, de causa desconhecida, os neurônios motores do corno anterior gradualmente atrofiam e desaparecem, tendo como conseqüência atrofia muscular, paralisias e morte. Os neurônios atróficos freqüentemente contêm abundante lipofuscina, daí o termo atrofia pigmentar.
4.Cromatólise central. A secção do axônio pode causar no neurônio alterações conhecidas como cromatólise central ou reação axonal: o corpo celular sofre tumefação, com desaparecimento dos corpúsculos de Nissl na porção central da célula e deslocamento do núcleo para a periferia. Estas alterações são geralmente reversíveis e interpretadas como um estado de metabolismo aumentado para favorecer a regeneração do axônio. Alteração semelhante pode ser observada em certas lesões crônicas do neurônio como, por exemplo, na pelagra.
5.Armazenamento. O citoplasma do neurônio pode acumular substâncias nas doenças de armazenamento. Em um grupo destas doenças, denominadas esfingolipidoses, o material acumulado é um esfingolípide, cujo tipo varia conforme a enzima lisossômica deficitária. São exemplos a doença de Tay-Sachs ou idiotia amaurótica familial (acúmulo de gangliósides) e a doença de Niemann-Pick (esfingomielina). Seja qual for a doença, os neurônios ficam volumosos, com contornos arredondados (aspecto abalonado) e o núcleo torna-se picnótico e deslocado para a periferia. O acúmulo pode provocar disfunção crônica e morte da célula.
6.Alteração neurofibrilar de Alzheimer. Esta alteração patológica ocorre em muitos neurônios, especialmente do hipocampo e córtex cerebral, na doença de Alzheimer, uma demência progressiva de causa desconhecida que afeta pacientes de ambos sexos, mais comumente após a 7a década. Porém é vista, em menor número de neurônios, como parte do processo normal de envelhecimento. Há deposição no citoplasma dos neurônios de uma proteína fibrilar, com características tintoriais de amilóide, que se impregna por prata, dando ao neurônio aspecto característico em chama de vela. O amilóide gradualmente ocupa lugar das organelas e do núcleo, causando morte da célula.
ALTERAÇÕES PATOLÓGICAS DAS CÉLULAS DA GLIA
ASTRÓCITOS
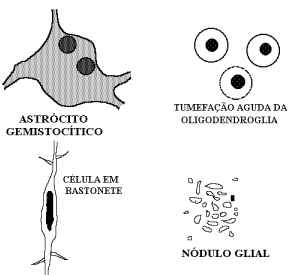
Os astrócitos têm como uma de suas funções principais a cicatrização do tecido nervoso após lesões diversas, papel semelhante ao dos fibroblastos em outros tecidos. Para isto os astrócitos, tanto protoplasmáticos quanto fibrosos, sofrem hipertrofia e hiperplasia. O citoplasma torna-se abundante, nítido, eosinófilo e homogêneo. O núcleo desloca-se para a periferia e, freqüentemente, observa-se binucleação. Estes astrócitos volumosos são denominados astrócitos gemistocíticos e são muito importantes, pois sua presença é indicação segura de lesão do tecido nervoso. (O nome deriva da palavra alemã gemästete, que significa engordado.) Os astrócitos gemistocíticos sintetizam copiosas quantidades da proteína específica dos astrócitos, a GFAP, que forma fibrilas no citoplasma destes. Ao longo de alguns meses, o volume do citoplasma diminue e as fibrilas se condensam, assumindo aspecto refringente, eosinófilo, que caracteriza o astrócito fibroso patológico (não confundir com o astrócito fibroso normal). Assim, um astrócito gemistocítico gradualmente se transforma em astrócito fibroso, cujo volume é menor, mas cujas fibrilas permanecem bem visíveis em HE. Após meses ou anos os astrócitos fibrosos podem diminuir em número e muitos desaparecem, mas as fibrilas gliais ficam permamentemente no tecido, agora em localização extracelular.
Denomina-se gliose o aumento no número e/ou volume dos astrócitos e deposição de fibrilas gliais no tecido nervoso central. Uma área de gliose recente contém muitos astrócitos gemistocíticos. Em uma área de gliose antiga o tecido tem aspecto ricamente fibrilar, sendo as fibrilas delicadas e eosinófilas. É o achado mais comum na vizinhança de infartos, hemorragias e abscessos, meses ou anos após a fase aguda da lesão.
OLIGODENDRÓGLIA
A oligodendróglia sofre por anóxia a tumefação aguda, que é a formação de um amplo vacúolo em volta do núcleo por entrada de água na célula. O aspecto é classicamente comparado ao de um ovo frito. A tumefação aguda é freqüente em material de autópsia e, neste caso, é interpretada como artefato decorrente de alterações metabólicas agônicas.
MICRÓGLIA
A micróglia, derivada do mesoderma, é a representante do sistema mononuclear fagocitário (ou sistema retículo-endotelial) no SNC. Sua transformação patológica mais freqüente é a célula grânulo-adiposa, que tem as características de um macrófago com citoplasma vacuolado. É a forma fagocitária ativa da micróglia, encontrada no tecido nervoso após vários tipos de lesão como infartos e hemorragias. A micróglia, que normalmente é uma célula alongada, sofre retração de seus prolongamentos, o citoplasma distribui-se ao redor do núcleo tomando forma arredondada e fagocitando restos celulares e baínhas de mielina degeneradas. Como o tecido nervoso é muito rico em lípides, os vacúolos coram-se em vermelho pelo escarlate R (corante para lípides). Após exercer sua função, as células grânulo-adiposas migram para os espaços perivasculares e ganham a luz de vênulas, sendo eliminadas por via sanguínea. Há evidência de que a maioria das células grânulo-adiposas provêm de monócitos do sangue e não de células microgliais pré-existentes.Outra forma reacional da micróglia é a célula em bastonete, encontrada nas encefalites crônicas. A micróglia mantém sua forma mas torna-se maior, com prolongamentos mais longos e retilíneos. Na HE, o que chama a atenção é o aumento do comprimento do núcleo, que assume forma em bastão, daí o nome da célula. Os prolongamentos são reconhecíveis só em impregnação pela prata. As células em bastonete são melhor observadas no córtex cerebral e no hipocampo, p.ex., na paralisia geral sifilítica. Em certas encefalites, as células microgliais ativadas podem formar pequenos aglomerados, os nódulos gliais, que, embora inespecíficos (ocorrem em encefalites por vírus, por protozoários como o Toxoplasma ou por fungos como a Candida), testemunham a natureza inflamatória do processo. Também, quando um neurônio morre acometido por um vírus (como na poliomielite), as células microgliais fagocitam ativamente os restos necróticos, formando um pequeno nódulo glial: o fenômeno é denominado neuronofagia.
EPÊNDIMA
Outra célula constituinte do tecido nervoso é a célula ependimária, que forma um epitélio cilíndrico simples, o epêndima, que reveste todo o sistema ventricular do encéfalo e o canal central da medula espinal. No feto as células ependimárias são ciliadas, perdendo os cílios progressivamente na vida pós-natal. Uma vez lesadas, p.ex., por agentes inflamatórios, não se regeneram, ficando o ventrículo naquele ponto revestido somente por astrócitos fibrosos, um aspecto conhecido como ependimite granulosa. As células ependimárias podem ainda originar tumores (ependimomas).
HIPERTENSÃO INTRACRANIANA
PRESSÃO NORMAL DO LÍQUIDO CÉFALO-RAQUIDIANO OU LÍQUOR (LCR).
A pressão normal do LCR, medida em decúbito lateral, varia entre 5 e 20 centímetros de água (cmH2O), sendo os valores mais próximos de 10 cmH2O na cisterna magna e de 15 cmH2O no fundo de saco lombar. A partir de 20 cmH2O (15 mmHg) fala-se em hipertensão do LCR ou hipertensão intracraniana (HIC). Na criança, a capacidade volumétrica da caixa craniana é expansível por não se terem ainda soldado as suturas. No adulto, o crânio é inexpansível, mas o encéfalo pode aumentar de volume focal ou difusamente em condições patológicas.
CAUSAS DA HIPERTENSÃO INTRACRANIANA
1.Lesões expansivas localizadas, como hematomas, abscessos e tumores podem aumentar o volume de um hemisfério cerebral. Geralmente o efeito de massa da lesão é amplificado pelo edema cerebral em torno da mesma.
2.Fatores que atuam difusamente, como anóxia sistêmica ou processos inflamatórios (meningites e encefalites) podem causar edema cerebral difuso e, portanto, aumento global do volume do encéfalo. Tanto num caso como noutro, a expansão cerebral aumenta a pressão intracraniana. Há uma escassa margem de segurança para evitar a hipertensão, representada pela quantidade de líquor, entre 100 a 150ml no adulto normal. Inicialmente a expansão cerebral é compensada por maior absorção do LCR. Em cérebros atróficos, com ventrículos dilatados e sulcos alargados, esta margem é correspondentemente maior. Esgotada a capacidade de compensação, a pressão intracraniana aumenta rapidamente. Fatores que atuam difusamente, como anóxia sistêmica ou processos inflamatórios (meningites e encefalites) podem causar edema cerebral difuso e, portanto, aumento global do volume do encéfalo. Tanto num caso como noutro, a expansão cerebral aumenta a pressão intracraniana. Há uma escassa margem de segurança para evitar a hipertensão, representada pela quantidade de líquor, entre 100 a 150ml no adulto normal. Inicialmente a expansão cerebral é compensada por maior absorção do LCR. Em cérebros atróficos, com ventrículos dilatados e sulcos alargados, esta margem é correspondentemente maior. Esgotada a capacidade de compensação, a pressão intracraniana aumenta rapidamente. Fatores que atuam difusamente, como anóxia sistêmica ou processos inflamatórios (meningites e encefalites) podem causar edema cerebral difuso e, portanto, aumento global do volume do encéfalo. Fatores que atuam difusamente, como anóxia sistêmica ou processos inflamatórios (meningites e encefalites) podem causar edema cerebral difuso e, portanto, aumento global do volume do encéfalo. Tanto num caso como noutro, a expansão cerebral aumenta a pressão intracraniana. Há uma escassa margem de segurança para evitar a hipertensão, representada pela quantidade de líquor, entre 100 a 150ml no adulto normal. Inicialmente a expansão cerebral é compensada por maior absorção do LCR. Em cérebros atróficos, com ventrículos dilatados e sulcos alargados, esta margem é correspondentemente maior. Esgotada a capacidade de compensação, a pressão intracraniana aumenta rapidamente.
CLÍNICA DA HIPERTENSÃO INTRACRANIANA
TRÍADE CLÍNICA DA HIPERTENSÃO INTRACRANIANA:
CEFALÉIA, VÔMITOS E EDEMA DE PAPILA
A hipertensão intracraniana caracteriza-se basicamente por cefaléia, vômitos e edema de papila. Os vômitos tendem a ser em jato. O edema de papila consiste em um borramento das margens da papila óptica ao exame oftalmoscópico. Ocorre porque a maior pressão intracraniana é transmitida ao redor dos nervos ópticos pelo manguito de meninges que os envolve, dificultando o retorno venoso. Isto leva inicialmente a uma congestão dos vasos da retina e depois ao edema de papila. Além da tríade clássica, podem associar-se confusão mental ou coma, crises convulsivas e sinais deficitários localizados, de acordo com a área atingida pela lesão, p. ex. hemiplegia, afasia e hemianopsia.
CONSEQÜÊNCIAS DA HIPERTENSÃO INTRACRANIANA
As complicações mais sérias da expansão do encéfalo são as hérnias, que consistem na insinuação sob pressão de linguetas de tecido cerebral em espaços exíguos, com compressão de estruturas vitais.
Principais hérnias encefálicas devidas à HIC:
1. de amígdalas cerebelares
2. de uncus temporal
3. supracalosa, ou do giro do cíngulo
A hérnia de amígdalas é a entrada das amígdalas cerebelares no foramen magno, um espaço só ocupado pela medula cervical. Decorre do aumento de volume de um ou ambos hemisférios cerebrais, e deslocamento caudal do tronco cerebral e cerebelo. A hérnia de amígdalas é bilateral. As amígdalas tomam forma cônica e comprimem o bulbo, causando disfunção geralmente irreversível do centro respiratório. Isto leva a parada respiratória. O tecido cerebelar herniado pode sofrer necrose por compressão vascular. Lesões expansivas no cerebelo podem também causar hérnia de amígdalas. A hérnia de uncus, também muito freqüente, corresponde à passagem do giro parahipocampal, ou de sua extremidade anterior, o uncus, para a fossa posterior através do orifício da tenda do cerebelo, onde se localiza o mesencéfalo. A hérnia de uncus é geralmente unilateral e conseqüente ao aumento de volume de um hemisfério cerebral por um hematoma, infarto, tumor, abscesso ou traumatismo. O edema em torno da lesão potencia grandemente a expansão do hemisfério e ajuda a pressionar o uncus para baixo, entre a margem livre da tenda do cerebelo e o mesencéfalo.
EFEITOS DA HÉRNIA DE UNCUS:
a) Compressão do nervo oculomotor (III), levando a midríase unilateral, grave sinal indicativo de sofrimento mesencefálico.
b) Distorção do mesencéfalo no sentido látero-lateral, com alongamento do eixo ântero-posterior. O alongamento do mesencéfalo leva a ruptura de vasos que cursam em direção ântero-posterior, com hemorragias na linha média do mesencéfalo, chamadas hemorragias de Duret. Estas propagam-se à ponte e ao diencéfalo e são sempre fatais.
c) Mais raramente, o mesencéfalo deslocado pode atingir a tenda do cerebelo do lado oposto, sofrendo secção da base do pedúnculo cerebral. Como aí passa o trato piramidal, ocorre hemiplegia ipsilateral à lesão cerebral (falso sinal de localização). Notar que a hemiplegia é ipsilateral porque o trato piramidal só cruza para o lado oposto na decussação das pirâmides, que ocorre abaixo do mesencéfalo, a nível do bulbo.
d) Compressão da artéria cerebral posterior, que circunda o mesencéfalo, levando a infarto no seu território. Estes infartos são chamados infartos calcarinos por incluir a área visual primária (área 17 de Brodmann, na fissura calcarina occipital), e são freqüentemente hemorrágicos, pois a compressão da artéria pode ser insuficiente para interromper completamente o fluxo sanguíneo. O infarto agrava o edema cerebral do hemisfério já comprometido por outra lesão.
A artéria cerebral posterior, derivada da bifurcação da A. basilar, cursa entre o mesencéfalo e o giro parahipocampal, sendo facilmente comprimida no caso de uma hérnia de uncus.
A hérnia do giro do cíngulo é sempre unilateral. É a mais rara e, como a hérnia de uncus, decorre do aumento de volume de um hemisfério cerebral. Pode haver deslocamento do giro do cíngulo para o lado oposto, insinuando-se entre a borda livre da foice do cérebro e o corpo caloso. A principal conseqüência é a compressão de uma ou ambas artérias cerebrais anteriores, que acompanham o corpo caloso, causando infarto hemorrágico deste território.
MORTE CEREBRAL E CÉREBRO DE RESPIRADOR
A pressão intracraniana pode, em casos muito graves, superar a própria pressão arterial sistólica. Quando isto ocorre, a circulação cerebral interrompe-se e sobrevém a morte cerebral.
O eletroencefalograma (EEG) passa a ser isoelétrico e os reflexos do tronco cerebral estão abolidos, embora os espinais possam permanecer.
A injeção de contraste radiológico na A. carótida interna não resulta em preenchimento dos vasos cerebrais.
Esses pacientes deixam de respirar mas, se a respiração for mantida por aparelhos, os batimentos cardíacos podem continuar, às vezes indefinidamente.
O cérebro no entanto está morto e sofre autólise in vivo:
* A cor torna-se difusamente arroxeada.
* Há perda da distinção entre substância branca e cinzenta.
* A consistência torna-se muito mole, até semifluida, lembrando pasta dental.
* O processo é mais intenso no cerebelo, onde a camada granulosa autolisa rapidamente e se destaca da camada molecular.
* Fragmentos de tecido cerebelar necrótico podem ser encontrados no espaço subaracnóideo espinal até o nível lombar, propelidos pela pressão intracraniana.
À autólise in vivo do encéfalo dá-se o nome de cérebro de respirador, pois é a manutenção artificial da vida que a possibilita. Esses cérebros não endurecem com a fixação e seu exame histológico é precário devido à intensa autólise.
Fonte:
http://www.bioturmas.hpg.ig.com.br/neuropatologia.html



