Estequiometria: Alguns conceitos básicos
A Estequiometria é um estudo realizado na química e envolve equações. A palavra estequiometria deriva do grego stoikheion, que significa elemento; e metriā, que significa medida. De uma forma básica, essa área de estudo segue os princípios da lei da conservação das massas, lei das proporções definidas e lei das proporções múltiplas.
A maior parte das reações químicas pode ser analisada sob o aspecto da estequiometria, pois elas combinam proporções de compostos químicos. O princípio da estequiometria está baseado no fato de a matéria não ser criada ou destruída, mas apenas transformada. Por isso, as reações envolvendo as proporções de cada elemento químico não se alteram durante ou depois das reações. Neste contexto, a estequiometria é empregada apenas para balancear as equações.
O cálculo estequimétrico permite que se descubra a quantidade de cada uma das substâncias envolvidas na reação química. Para realizar esse tipo de cálculo, é preciso escrever a equação, balancear a equação e estabelecer as proporções.
Nesse tipo de cálculo, é importante acertar os coeficientes estequiométricos. Todas as grandezas da reação devem ser consideradas.
Também é importante destacar que nos cálculos estequiométricos o grau de pureza e o rendimento das substâncias devem ser avaliados, já que as possíveis impurezas devem ser descontadas.
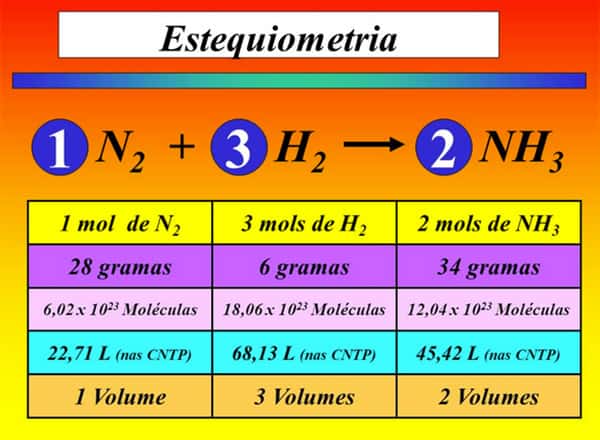
Leis importantes para o cálculo estequiométrico
Todas as reações químicas devem seguir as três leis descritas abaixo:
Lei de Lavoisier: em uma reação química, que acontece em um sistema fechado, a soma das massas dos reagentes será igual à soma das massas dos produtos.
Lei de Gay-Lussac: em condições semelhantes de temperatura e pressão, os volumes dos gases que fazem parte de uma reação estabelecem uma relação de números inteiros.
Lei de Proust: uma substância tem sempre a mesma proporção dos elementos que a formam.
Lembre-se que o objetivo da estequiometria é calcular e relacionar as quantidades de reagentes e produtos em uma reação química. Sendo assim, os cálculos da estequiometria sempre partirão de uma análise da presença de reagentes e produtos existentes no meio reacional. É possível resolver os problemas com regras de três simples, empregando os dados que já estão disponíveis na primeira linha da equação, e os dados que precisam ser obtidos na segunda linha. A regra de três estabelece uma proporção.
Veja também:
Cálculo estequiométrico com geração de energia


